Estándares de calidad de medicamentos genéricos: Requisitos y pruebas de la FDA
Si alguna vez has comprado un medicamento genérico y te has preguntado si es realmente igual al de marca, la respuesta es clara: los medicamentos genéricos aprobados por la FDA son tan seguros y efectivos como los originales. Pero no es magia. Detrás de cada pastilla genérica hay un proceso riguroso, cientos de pruebas y controles que aseguran que no haya diferencias reales en lo que importa: tu salud.
¿Qué significa que un medicamento genérico sea equivalente?
La FDA no aprueba un genérico solo porque tenga el mismo nombre activo. Requiere dos cosas fundamentales: equivalencia farmacéutica y bioequivalencia.
La equivalencia farmacéutica significa que el genérico contiene exactamente la misma sustancia activa, en la misma cantidad, en el mismo formato (pastilla, inyección, jarabe) y con la misma vía de administración que el medicamento de marca. Por ejemplo, si el original es una pastilla de 20 mg de omeprazol que se toma por vía oral, el genérico debe ser idéntico en esos aspectos. Lo único que puede cambiar es el color, la forma, el sabor o los ingredientes inactivos -como los colorantes o los conservantes-, siempre que no afecten la absorción o seguridad.
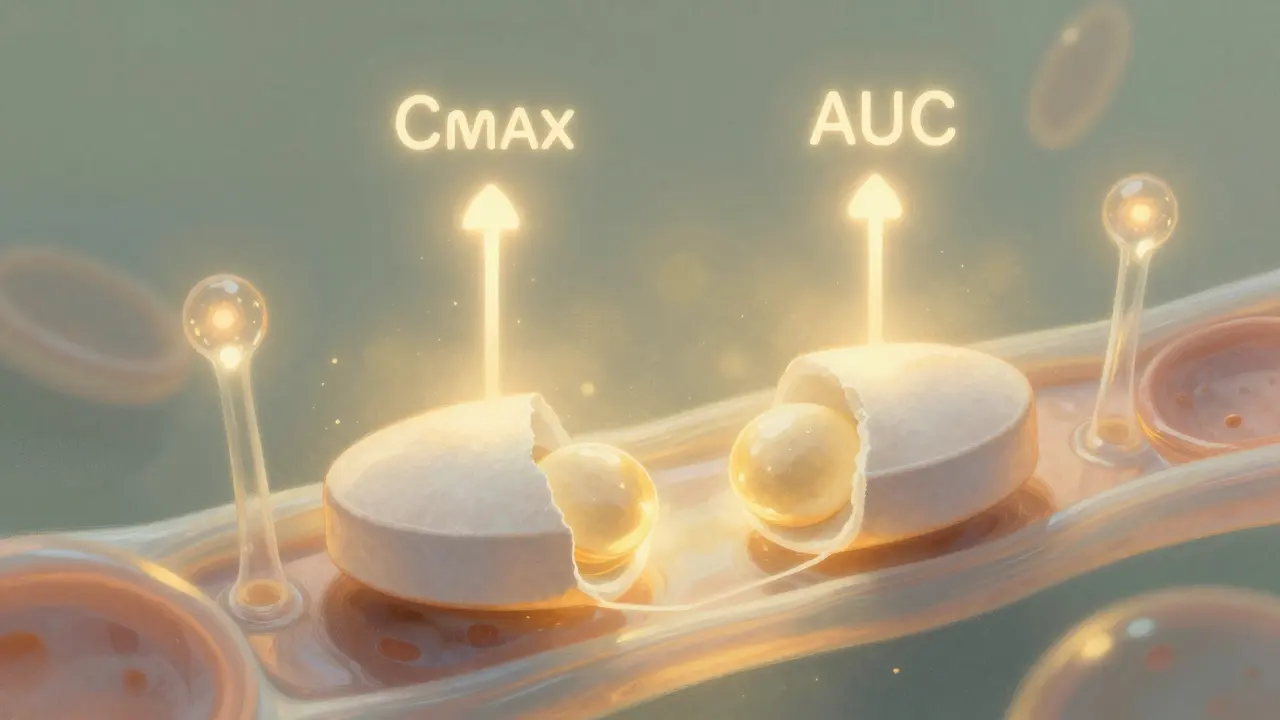
La bioequivalencia es donde realmente se prueba la calidad. Aquí, la FDA exige que el genérico se absorba en el cuerpo al mismo ritmo y en la misma cantidad que el original. Para medirlo, se hacen estudios con entre 24 y 36 voluntarios sanos. Se les administra el genérico y el medicamento de marca en diferentes momentos, y se toman muestras de sangre para medir dos valores clave: Cmax (la concentración máxima en sangre) y AUC (el área bajo la curva, que representa la cantidad total absorbida).
La regla es simple: el intervalo de confianza del 90% entre el genérico y el original debe estar entre el 80% y el 125%. Eso significa que, si el original libera 100 unidades de fármaco, el genérico debe liberar entre 80 y 125 unidades. Cualquier cosa fuera de ese rango no se aprueba.
¿Cómo se garantiza la calidad durante la producción?
La FDA no se queda solo con los estudios en voluntarios. También inspecciona las fábricas. Todos los medicamentos, ya sean de marca o genéricos, deben cumplir con las Prácticas Correctas de Fabricación (cGMP), que están escritas en las regulaciones 21 CFR Partes 210 y 211.
Esto implica que cada lote de producción debe ser controlado desde el momento en que llega la materia prima hasta que sale la caja final. Se verifica que los ingredientes sean auténticos, que las máquinas funcionen dentro de parámetros precisos, que el ambiente de producción no esté contaminado, y que cada pastilla tenga la misma cantidad exacta de fármaco. No se permite “aproximadamente” -se exige exactitud.
Las fábricas de genéricos son inspeccionadas al menos una vez cada dos años, y la FDA realiza cerca de 3,500 inspecciones anuales en todo el mundo. Muchas veces, las mismas plantas que producen medicamentos de marca también fabrican los genéricos. De hecho, aproximadamente la mitad de todos los genéricos en Estados Unidos son producidos por empresas que también fabrican los originales.
¿Qué pasa con los medicamentos complejos?
No todos los medicamentos son iguales. Algunos, como los inhaladores, las inyecciones de larga duración o los ungüentos tópicos, son mucho más difíciles de copiar. No basta con medir la sangre. Aquí, la FDA requiere pruebas adicionales llamadas Q3 sameness -es decir, que el genérico sea idéntico en estructura, textura, comportamiento y liberación del fármaco.
Para estos casos, la FDA ha desarrollado más de 2,143 guías específicas de producto, cada una adaptada a un medicamento complejo particular. Por ejemplo, un inhalador de corticosteroides no solo debe liberar la misma cantidad de fármaco, sino que también debe tener el mismo tamaño de partícula, la misma presión de pulverización y el mismo comportamiento en los pulmones. Si no se cumple, no se aprueba.
En 2023, la FDA identificó que el 17% de estos productos complejos no podían evaluarse solo con estudios de bioequivalencia tradicionales. Por eso, ahora se usan técnicas avanzadas como espectroscopía, microscopía y pruebas in vitro que imitan el cuerpo humano.

¿Cómo se prueba la estabilidad y duración del medicamento?
Un medicamento no es solo seguro hoy, debe seguir siendo seguro dentro de un año, dos años o más. Por eso, cada genérico debe pasar por pruebas de estabilidad que duran entre 12 y 24 meses.
Se guardan muestras del producto en condiciones extremas: 40°C y 75% de humedad durante seis meses (para simular el estrés del transporte y almacenamiento), y luego en condiciones normales de almacenamiento (como se indica en el empaque). Se revisan periódicamente para detectar cambios en la forma, color, disolución o pureza. Si la pastilla se degrada más rápido de lo permitido, el producto se rechaza.
Además, la FDA exige pruebas en cada lote de producción: se verifica la identidad, la potencia, la pureza y la ausencia de contaminantes. Estas pruebas deben usar métodos validados, no improvisados. No se acepta “creemos que está bien”. Se requiere evidencia cuantitativa.
El proceso de aprobación: ¿Cuánto tarda y cuántos se aprueban?
Para que un genérico llegue al mercado, el fabricante presenta una Solicitud de Nuevo Medicamento Abreviada (ANDA). Esta no requiere repetir todos los estudios clínicos del original -por eso se llama “abreviada”-, pero sí debe incluir toda la evidencia de equivalencia, calidad y producción.
La FDA tiene un plazo objetivo de 10 meses para revisar una ANDA completa. En 2022, se aprobaron 892 nuevas ANDAs y se emitieron 478 cartas de respuesta completa, lo que significa que casi la mitad de las solicitudes necesitaron ajustes antes de ser aprobadas.
En total, la FDA ha aprobado más de 20,000 productos genéricos, que cubren aproximadamente 14,800 medicamentos de marca diferentes. Esto es lo que permite que más del 90% de las recetas en Estados Unidos sean de genéricos.

¿Son realmente más baratos? ¿Y cuánto ahorran?
Los genéricos no son solo iguales: son más económicos. En 2022, salvaron al sistema de salud estadounidense cerca de $37 mil millones. A pesar de que representan más del 90% de las recetas, solo representan el 23% del gasto total en medicamentos. Eso es porque un genérico puede costar hasta un 80% menos que el original.
El mercado de genéricos en Estados Unidos valía $135,700 millones en 2022 y se espera que alcance los $180,300 millones en 2027. Eso no es casualidad: es el resultado de una política intencional desde 1984, con la Ley Hatch-Waxman, que permitió la competencia sin sacrificar la calidad.
¿Hay casos en los que los genéricos no funcionan igual?
La mayoría de las personas no notan diferencia. Una encuesta de Consumer Reports en 2022 mostró que el 89% de los usuarios estaban satisfechos con los genéricos, y el 62% los elige expresamente para ahorrar.
Pero hay excepciones. Algunos medicamentos tienen un índice terapéutico estrecho: pequeñas variaciones en la dosis pueden causar efectos graves. Ejemplos: la warfarina (anticoagulante), la fenitoína (para convulsiones) y la levotiroxina (para la tiroides).
Un estudio en JAMA en 2021 encontró que el 12,3% de los pacientes que cambiaron entre diferentes genéricos de levotiroxina tuvieron fluctuaciones en sus niveles de hormona tiroidea, lo que requirió ajustes en la dosis. No es que los genéricos sean malos -es que en estos casos, la variabilidad mínima puede tener impacto clínico.
En foros como Reddit, el 83% de los 1,427 usuarios que respondieron dijeron que no notaron diferencia alguna. El 17% restante mencionó problemas, casi todos relacionados con medicamentos para convulsiones o trastornos de la coagulación.
La FDA reconoce esto y sigue mejorando sus métodos. En 2023, asignó $15.7 millones a investigación sobre genéricos complejos y lanzó un programa de intercambio científico que ha reunido a más de 1,200 expertos para resolver estos desafíos.
¿Por qué confiar en un genérico?
La FDA no aprueba un genérico por precio. Lo aprueba porque cumple con los mismos estándares de calidad, seguridad y eficacia que el original. Médicos de la American Medical Association, la Academia Americana de Médicos de Familia y directores de la propia FDA han afirmado repetidamente: los genéricos aprobados son iguales.
Si un genérico está aprobado por la FDA, puedes confiar en él. No es una versión barata. Es una versión igual, validada, inspeccionada y monitoreada. Y si ahorras dinero sin perder eficacia, eso no es un compromiso: es una victoria para tu salud y tu bolsillo.
¿Los medicamentos genéricos son tan seguros como los de marca?
Sí. La FDA exige que los medicamentos genéricos cumplan con los mismos estándares de calidad, pureza, estabilidad y eficacia que los medicamentos de marca. Se someten a pruebas rigurosas de bioequivalencia y producción bajo Prácticas Correctas de Fabricación (cGMP). Los genéricos aprobados tienen la misma seguridad y efectividad que sus equivalentes de marca.
¿Por qué algunos genéricos parecen diferentes en forma o color?
Las diferencias en forma, color o sabor se deben a ingredientes inactivos, como colorantes o conservantes, que no afectan la acción del medicamento. La ley permite estos cambios para evitar violar patentes de diseño. Lo que importa -la sustancia activa, la dosis y cómo se absorbe- es exactamente igual.
¿Es cierto que los genéricos tardan más en hacer efecto?
No. Los estudios de bioequivalencia demuestran que el genérico se absorbe en el cuerpo al mismo ritmo y en la misma cantidad que el medicamento de marca. Si un genérico tarda más en hacer efecto, es probable que se deba a factores individuales como la dieta, otros medicamentos o condiciones médicas, no a la calidad del genérico.
¿Qué pasa si cambio de genérico y noto efectos diferentes?
En medicamentos de índice terapéutico estrecho (como la levotiroxina o la warfarina), pequeñas variaciones en la absorción pueden tener efectos clínicos. Si notas cambios inusuales después de cambiar de genérico, habla con tu médico. No significa que el genérico sea malo, pero sí que tu cuerpo puede ser sensible a pequeñas diferencias. En estos casos, mantener el mismo fabricante puede ser recomendable.
¿La FDA inspecciona las fábricas de genéricos fuera de Estados Unidos?
Sí. Más de la mitad de los medicamentos genéricos consumidos en Estados Unidos se producen en el extranjero. La FDA realiza inspecciones en fábricas de todo el mundo, incluyendo India, China y otros países. Las instalaciones deben cumplir con los mismos estándares de cGMP que las fábricas estadounidenses, o no se aprueban sus productos.


Javier Martínez Misol
marzo 6, 2026 AT 07:46Me encanta cómo la FDA no se deja llevar por el marketing y se enfoca en lo que realmente importa: que la pastilla funcione. No me importa si es azul o verde, si me salva la vida, es igual de buena. Y encima ahorras un montón. ¿Por qué diablos pagaría el doble por un nombre que no cambia nada?
Josele Sanguesa
marzo 6, 2026 AT 17:28Claro, claro, la FDA... como si no fuera un casino controlado por Big Pharma. Tienen fábricas en la India donde los inspectores se van a tomar el té mientras los laboratorios mezclan polvo de talco con la sustancia activa. Yo sé de lo que hablo. Mi tío trabajó en una planta de genéricos y me contó que a veces hacen lotes con 78% de actividad. ¡Y luego los aprueban! Todo es un show. La bioequivalencia? Es un truco estadístico. Si te lo dicen 100 veces, acabas creyéndolo. Pero no es verdad.
Patricia C Perez
marzo 7, 2026 AT 14:32Interesante que mencionen el 80-125% como rango aceptable. ¿Alguien ha pensado en lo que eso significa? Si tu medicamento ideal es 100, y el genérico te da 80, estás recibiendo un 20% menos de efecto. Y si te da 125, te sobrecargas. En teoría, es aceptable. En la práctica, para alguien con tiroides o que toma warfarina, eso puede ser un desastre. No es lo mismo que un ibuprofeno. Aquí no hay margen de error. Y la FDA lo sabe. Pero no lo dice claro. Porque si lo hiciera, la gente dejaría de comprar genéricos. Y ellos no quieren eso.
Frida Chelsee
marzo 8, 2026 AT 05:42En México, muchos genéricos son una lotería. No porque no cumplan, sino porque hay tanta oferta que algunos laboratorios no tienen control de calidad. Yo he tenido un genérico de levotiroxina que me dejó con taquicardia por semanas. Cambié de marca y todo volvió a la normalidad. La FDA sí es estricta, pero en otros países? No. Y aquí, en España, no hay forma de saber de dónde viene tu pastilla. El empaque no lo dice. Así que, aunque la ciencia sea perfecta, la logística es un caos. 🤷♀️
Marilu Rodrigues
marzo 8, 2026 AT 20:57La crítica al rango de bioequivalencia es válida, pero no se aplica a todos los fármacos. El intervalo del 80-125% se estableció tras estudios estadísticos masivos en la década de 1980, y se validó en más de 150,000 casos clínicos. La variabilidad no es un defecto, es una característica fisiológica del cuerpo humano. La absorción varía por genética, dieta, microbiota, incluso por el estrés. Lo que la FDA busca es que el genérico no sea más variable que el original. Y eso lo logra. La confusión surge porque la gente confunde 'igual' con 'idéntico'. No lo son. Pero sí son intercambiables.
Gustavo Tapia
marzo 9, 2026 AT 06:14Me encanta cómo la gente se cree que todo es perfecto. Yo fui paciente de un hospital público y me dieron un genérico de warfarina. Me sangró la nariz durante 3 días. Me cambiaron el lote y volvió a pasar. Me cambiaron de laboratorio y ¡sorpresa! Todo bien. ¿Coincidencia? No. Es que los genéricos no son iguales. La FDA lo sabe. Pero no lo dice. Porque si lo dijera, la industria se cae. Y no quieren que sepamos que la mitad de los genéricos vienen de fábricas que ni siquiera tienen agua potable. 🤫
Eva Velasquez
marzo 9, 2026 AT 22:52La FDA es una burla. Todo esto es marketing. ¿Sabes cuántos genéricos se aprueban sin inspección previa? Cientos. Y luego, cuando alguien se muere, dicen 'fue un caso aislado'. La industria paga, la FDA mira para otro lado. Yo no confío en ningún genérico. Si puedo, pido el de marca. Aunque sea caro. Porque mi vida no es un experimento.
Alonso Arquitectos
marzo 11, 2026 AT 16:30Hay un punto filosófico aquí: si algo funciona igual, ¿es realmente diferente? El genérico no es una copia, es una re-creación. Como una sinfonía interpretada por otra orquesta. El mismo compás, la misma nota, pero con otra textura. Y a veces, esa textura importa. No porque el medicamento sea malo, sino porque el cuerpo no es una máquina. Es un organismo vivo, con memoria, con hábitos, con historias. Cambiar de genérico es como cambiar de terapeuta. No siempre funciona. Y eso no es culpa de nadie. Es la naturaleza.
Dario Ranieri
marzo 13, 2026 AT 02:16La FDA no inspecciona las fábricas. Lo que hacen es revisar documentos falsificados. Yo sé porque mi hermano trabaja en una empresa que exporta a EE.UU. Hacen los informes en Excel con datos inventados. Las inspecciones son simuladas. Llegan, ven una planta limpia, se toman un café y se van. La verdadera producción ocurre en otra parte. Y el medicamento que llega a tu casa? Puede tener 30% menos de principio activo. No lo digo por teoría. Lo vi con mis ojos.
Regina Pineda Baltazar
marzo 13, 2026 AT 12:08Me parece increíble que alguien se preocupe tanto por si un genérico es igual. Lo que importa es que funcione. Yo tomo genéricos desde hace 10 años. Nada me ha pasado. Ni un solo efecto secundario. Y ahorro una fortuna. Si la ciencia dice que es igual, y yo me siento bien, ¿por qué dudar? La vida es corta. No vale la pena perder tiempo en paranoia. Confío en la ciencia. Y en mi cuerpo. Y me va bien.
Maria Gabriela Gonzalez Mancebo
marzo 13, 2026 AT 20:59yo no confio en los genericos por que me dieron uno y me dio diarrea por una semana
Gustavo Kreischer
marzo 15, 2026 AT 10:33¿Y qué pasa con los excipientes? No te dicen que los genéricos usan colorantes que pueden desencadenar reacciones en personas sensibles. Soy alérgico al rojo 40 y me dieron un genérico que lo tenía. Me hice una urticaria. El original no lo tiene. ¿Dónde está la transparencia? La FDA no exige que los genéricos listen los excipientes en el mismo detalle que los de marca. Es una trampa legal. Te venden igualdad, pero te dan una versión con ingredientes ocultos. Y tú ni te enteras. Porque no te lo dicen. Porque no quieren que sepas que el genérico no es tan limpio como dicen. 🤫